Servicios globales
Identificador único de dispositivo (UDI)
El 24 de septiembre de 2013, la Food and Drug Administration (FDA) de Estados Unidos emitió una norma definitiva que requiere que la mayoría de dispositivos médicos se distribuyan en Estados Unidos con un identificador único de dispositivo (UDI). El sistema UDI facilita la identificación, trazabilidad y seguimiento del dispositivo médico a través de su distribución y uso. La norma requiere que la información del producto pertenece a los dispositivos introducidos en la Base de Datos Global de Identificador Único de Dispositivo (GUDID) de la FDA.
Además, la norma también requiere que se introduzca un formato de fecha nuevo y estandarizado en todas las etiquetas de dispositivos médicos.
Masimo ha actualizado su etiquetado para cumplir con la normativa UDI y estándares GS1.
Si tiene preguntas más allá de estas preguntas frecuentes, póngase en contacto con Servicio al cliente:
EE. UU.: customerorders@masimo.com
Fuera de EE. UU.: emeasales@masimo.com
1. ¿Qué es el UDI?
Un identificador único de dispositivo (UDI) es una serie de caracteres numéricos o alfanuméricos basada en un estándar de codificación internacional que identifica de forma adecuada un dispositivo en el punto de distribución y en el punto de uso. Un UDI se compone de:
- Un identificador de dispositivos, el GTIN (Número de elemento de comercio internacional): una porción obligatoria y fija de un UDI identifica la versión específica o modelo de dispositivo y el etiquetador de ese dispositivo; y
- un identificador de producción: una porción condicional y variable de un UDI que identifica uno o más de los siguientes cuando se incluyen en la etiqueta del dispositivo:
- el lote o partida de producción en el que se fabricó un dispositivo;
- el número de serie del dispositivo específico;
- la fecha de caducidad de un dispositivo específico; o
- la fecha en que se fabricó un dispositivo específico.
Masimo utiliza GS1 como su agencia acreditada para asignar códigos de barras y estructuras de código de barras.
Tenga en cuenta que cualquier producto que NO esté clasificado como dispositivo médico no requiere que contenga un código de barras.
2. ¿Quién tiene que cumplir con las normativas UDI?
Todas las empresas de dispositivos médicos deben cumplir con las normativas UDI.
3. ¿Cuál es el calendario de implementación para cumplir con las normativas UDI?
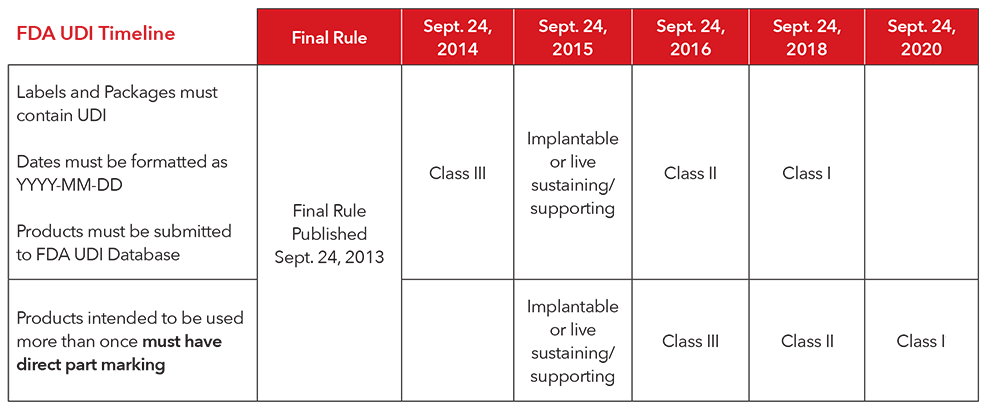
4. ¿Cómo cumple Masimo con la UDI?
Masimo distribuye productos de clase II y unos pocos de clase I. Masimo ha actualizado su etiquetado para cumplir con la normativa UDI y estándares GS1.
Tenga en cuenta que cualquier producto que NO esté clasificado como dispositivo médico no requiere que contenga un código de barras.
5. ¿Cómo será mi etiqueta UDI y el marcado directo de la pieza?
A continuación, encontrará algunos ejemplos:
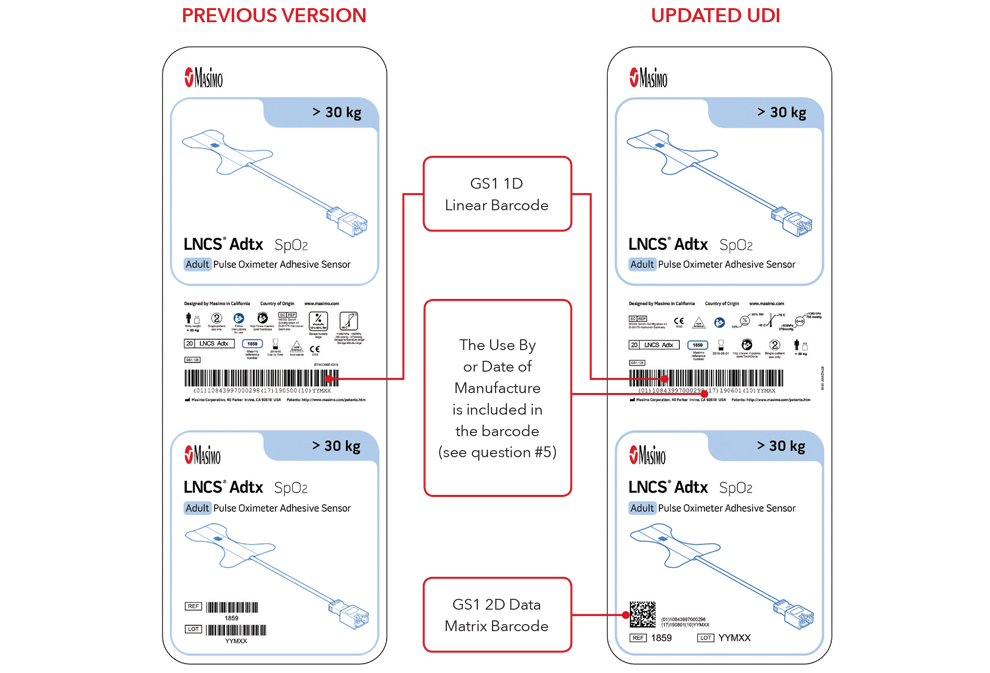
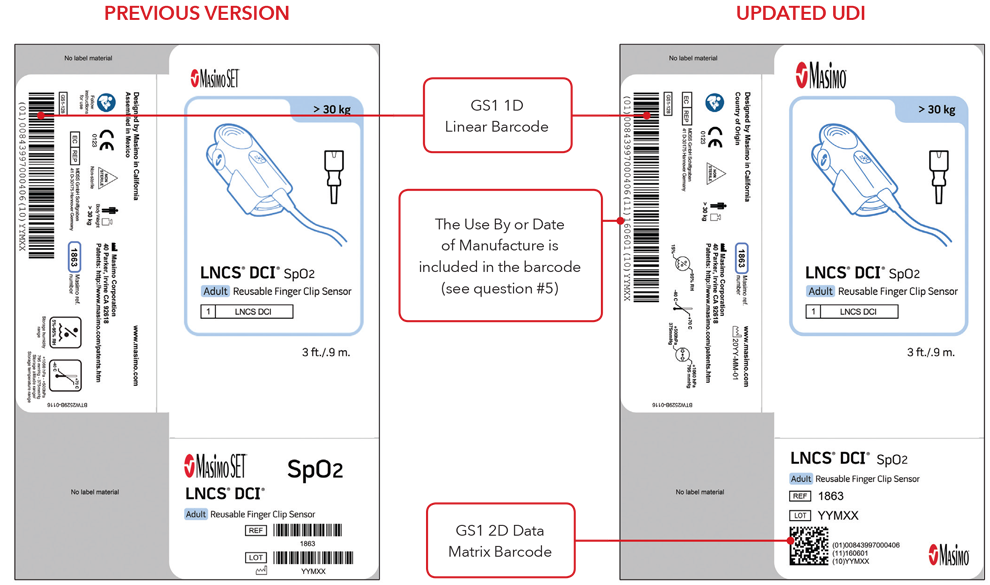
- Etiquetas de la caja del sensor con la versión anterior y etiquetas UDI actualizadas
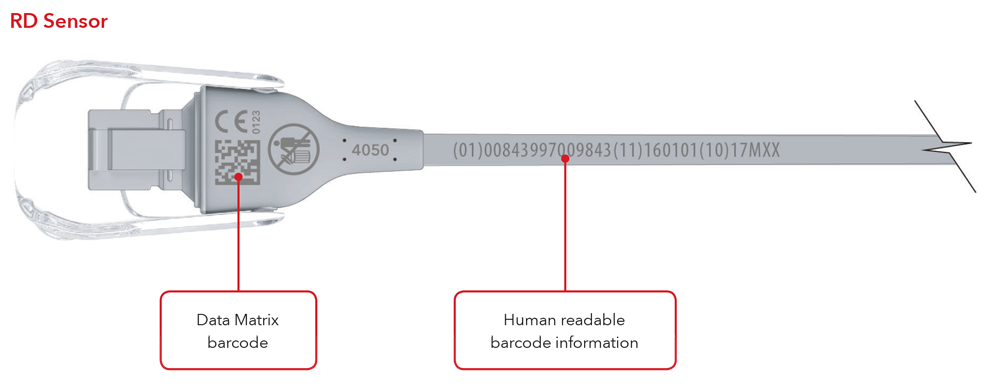
- Sensor con marcado directo de la pieza
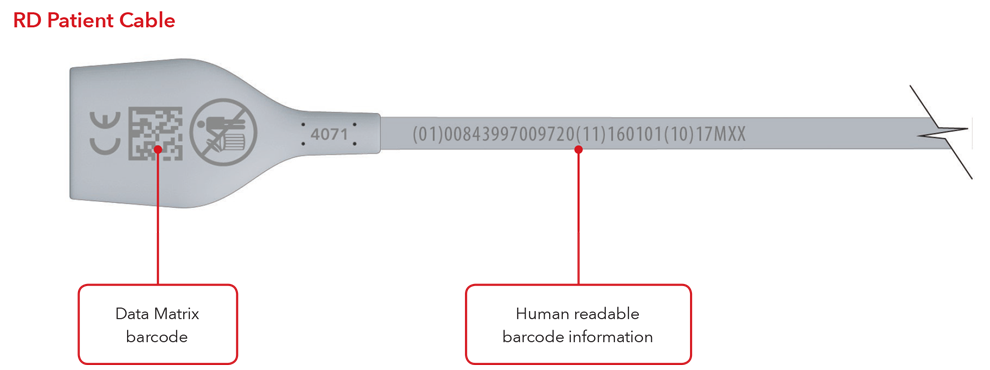
- Cable con marcado directo de la pieza
Nota: Dependiendo del tipo de producto, la etiqueta contendrá una de dos fechas. Para productos con fecha de caducidad, esta aparecerá como AAAA-MM-DD debajo del símbolo de caducidad, y también se codificará como AAMMDD precedida por la identificación de producción (17) dentro de los códigos de barras GS1 y 2D. Para productos sin fecha de caducidad, la fecha de fabricación aparecerá como AAAA-MM-DD junto con el símbolo de fecha de fabricación, y también se codificará como AAMMDD precedida por la identificación de producción (11) dentro de los códigos de barras GS1 y 2D.
Ejemplos de etiquetas de cajas de sensores
Ejemplos de sensor y cable con marcado directo de la pieza
6. ¿Qué es un número de elemento de comercio internacional (GTIN)?
Un GTIN es un número de identificación internacional único GS1 utilizado para identificar un "elemento de comercio". Los GTIN se asignan por propietario de la marca (etiquetador) del producto y se utilizan para identificar productos a medida que se desplazan en la cadena de suministro internacional al usuario final, como un hospital. Si no está utilizando actualmente el sistema GS1 con GTIN para gestionar sus productos, deberá obtener los GTIN para los productos que está comprando.
Para obtener más información sobre los GTIN, póngase en contacto con GS1 en: https://www.gs1us.org/what-we-do/standards.
7. ¿Cómo obtengo el/los GTIN de producto?
Correo electrónico de Servicio al cliente de Masimo:
EE. UU.: customerorders@masimo.com
Fuera de EE. UU.: emeasales@masimo.com
Incluya su ID de cliente y el/los números de pieza de producto en el correo electrónico.
8. Actualmente, introduzco o escaneo el lote Masimo o los códigos de barras REF en la etiqueta. ¿Debería esperar alguna interrupción?
Sí. Los códigos de barra del lote o referencia de la etiqueta se eliminarán y reemplazarán con texto y ya no se podrán escanear. Para información sobre el lote, deberá escanear el código de barras de GS1 o localizarlo junto al símbolo del lote en la etiqueta. La información de referencia puede identificarse en el GTIN correspondiente. Para obtener más información sobre los GTIN, consulte la pregunta 6 anterior.
9. ¿Cambiarán los números de producto de Masimo con la implementación del etiquetado UDI?
No, los números de producto de Masimo seguirán siendo los mismos.
10. ¿Qué es el formato de fecha nuevo estandarizado y cuándo entra en vigor?
La regla del UDI adoptó el formato de fecha estandarizado AAAA-MM-DD en etiquetas de dispositivos. Las fechas en etiquetas estarán en el nuevo formato no más tarde que la fecha en que la etiqueta del dispositivo deba incluir un UDI. Para obtener más información sobre el calendario de implementación, consulte la pregunta 3 anterior.
11. ¿Proporcionará Masimo información del producto en línea?
La GUDID es una base de datos en la que pueden realizarse búsquedas públicamente que contiene la porción de identificación del dispositivo (DI) para todos los dispositivos médicos, así como cualquier otra información de producto solicitada. Todas las empresas de dispositivos médicos deben enviar la información de DI al GUDID. Masimo ha comenzado a completar la GUDID y se asegurará de que todos los productos se añadan de acuerdo con el calendario de implementación del UDI o antes de su finalización.
12. ¿Y los inventarios existentes? ¿Los fabricantes tienen que volver a marcarlos?
No, hay dos excepciones para inventarios existentes:
- Los dispositivos que estén en distribución comercial previa a la fecha de cumplimiento aplicable no tienen que cumplir con la norma final.
- Los dispositivos que estén en fabricados y etiquetados previamente a la fecha de cumplimiento también están exentos de este cumplimiento. Sin embargo, esta excepción caduca 3 años después de la fecha de cumplimiento aplicable.
13. ¿Todos los dispositivos deben estar marcados directamente con sus UDI?
No. La regla solo requiere el marcado directo para dispositivos médicos reutilizables que necesiten reprocesarse (esterilización/limpieza de alto nivel) antes de su reutilización.
Para obtener más información sobre el calendario de implementación del marcado directo, consulte la pregunta 3 anterior.
Para más información sobre el sistema UDI, visite Unique Device Identification (UDI) (Identificador único de dispositivo) en el sitio web de la FDA:
http://www.fda.gov/MedicalDevices/DeviceRegulationandGuidance/UniqueDeviceIdentification/
Si tiene alguna pregunta adicional sobre cómo Masimo cumple con la normativa UDI, póngase en contacto con el servicio de atención al cliente de Masimo en:
EE. UU.: customerorders@masimo.com
Fuera de EE. UU.: emeasales@masimo.com
PLCO-008044/ PLMM-12790A-0326 EN- PLMM-10045D